医疗网络,5月7日,国家药品监督管理局发布通知,全国医疗器械抽样检验工作启动,抽样方案发布。
5月6日,国家药品监督管理局官网发布《国家药品监督管理总局综合司关于印发2019年国家
医疗器械抽样检验项目的通知》(以下简称《通知》),于年发布《国家医疗器械抽样检验项目》。2019年至省、自治区、直辖市药品监督管理局。
这意味着,按照国家药品监督管理局发布的“2019年全国医疗器械抽样调查实施通知”的要求,医疗器械抽样调查工作已经全面展开。
国家药品监督管理局今天的通知要求,省、自治区、直辖市人民政府应当组织有关检验机构执行医疗器械强制性标准,并按照国家抽样检验的要求进行注册或者备案。2019年医疗器械离子计划(中央补助地方项目)和2019年国家医疗器械抽样检查计划(国家预算项目)。产品技术要求(注册产品标准)进行检验工作。
对上述两种产品检验方案进行了梳理,共列入抽检范围的医疗器械产品有59种,包括中央资助的地方项目中的病人监护仪、心电图机、腹部穿刺仪、血糖计等49种产品。以及国家预算项目、移动X射线机及多类型检测试剂盒等10种产品。
根据产品抽样项目的确定原则,上述产品检验方案表明,任何抽样检验项目均被判定为不合格,则本次抽样检验的综合结论是不合格的。 产品抽样检验的目的是加强对上市后医疗器械产品的质量监督。据报道,2019年3月5日至7日,在2019年在广州召开的全国医疗器械抽样检验座谈会上,国家局医疗器械监督管理司司长王者雄表示,我国医疗器械抽样检验工作仍存在诸多问题和挑战。要求各单位认真组织、整合国家医疗器械抽样检验资源,规范医疗器械抽样检验行为,严格监督、做好不合格品召回工作。工作总结的信息发布和报告。
国家药品监督管理局抽查通知书还明确了复核工作和推荐复核机构名单。
为保证复验的有效性,申请人可从2019年国家医疗器械检验复验机构推荐的名单中进行选择。逾期不申请复审的,视为申请人同意复审结果,审查机构不再受理复审申请。
同时,对异议投诉,通知显示抽样单位或者有标记的生产企业对检验方法、判断依据等有异议,无法在收到检验报告之日起七个工作日内通过复验核实,提出异议和申诉的书面申请,应当向所在地省局提出,并提交有关的证明材料。
省级局接到申请后2个工作日内,向国家医疗器械抽样检验信息系统提出投诉,15个工作日内进行调查核实,确认核实结果,并向技术部门提出处理意见。中国食品药品监督管理局监督中心。省有关部门不进行调查检查,不提出核查结果和处理建议的,将退还有关资料。

 吸引器
吸引器 高频电刀
高频电刀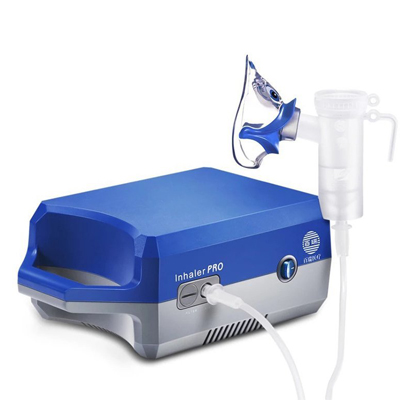 雾化器
雾化器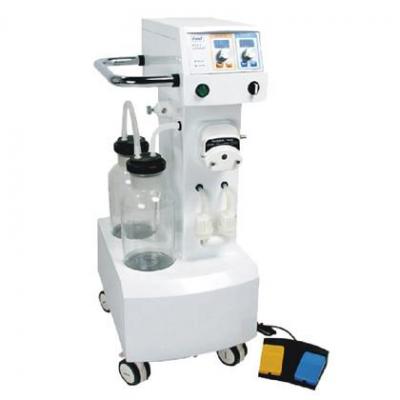 吸脂机
吸脂机 洗胃机
洗胃机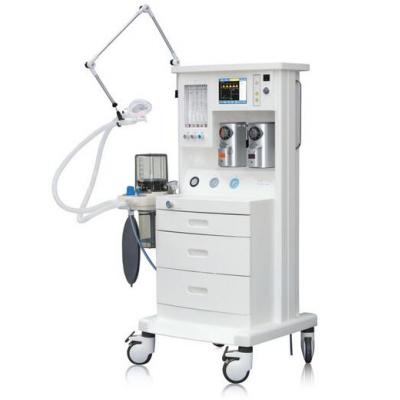 麻醉机
麻醉机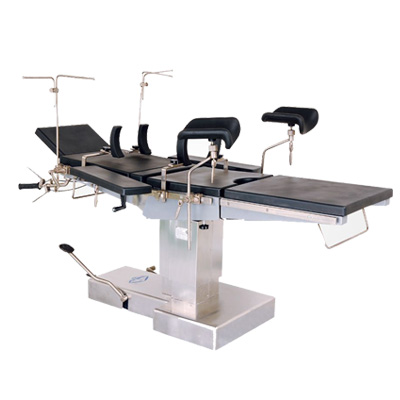 手术台
手术台 无影灯
无影灯