上海市药品监督管理局发布了《关于医疗器械生产企业跨地区飞行检查的通知》。其中四人因严重缺陷被停工,一人主动提出停产整顿报告。
发现的问题及处理措施
(1)飞行检验发现,上海苏州
医疗器械吸引器有限公司、上海奥新医疗科技有限公司、上海美建医疗器械制造有限公司、上海盛昌光电科技有限公司不符合医疗器械生产质量管理标准的有关规定,生产质量管理体系存在严重缺陷。以上四家企业应暂停生产整改,评估产品安全风险。如有可能造成隐患,应按照《医疗器械召回管理办法》的规定及时召回相关产品。
其中,上海盛昌光电科技有限公司涉嫌违反“医疗器械监督管理条例”的有关规定,依法移交检查部门查处。
(2)飞行检查发现上海普益医疗器械有限公司不符合医疗器械生产质量管理标准的有关规定。生产质量管理体系存在严重缺陷。企业主动提出停产报告,要求整改。企业涉嫌违反“医疗器械监督管理条例”的有关规定,依法移送检验部门查处。企业应当按照《医疗器械召回管理规定》,对产品安全风险进行评估,及时召回相关产品。
(3)飞行检查发现,上海华新医疗核仪器有限公司的医疗设备产品停产一年以上,未生产同类产品。企业必须在复产前向我局书面报告,经检查符合要求后方可复产。
(4)在进行飞行检查时,上海诺港生物技术有限公司的生产地址正在翻新。企业恢复生产前,应当书面向本部门报告,经审核合格后恢复生产。
上海市药品监督管理局已要求有关监管部门督促有关企业按照上述办法实施整改措施,对违法违规行为依法严格查处,及时消除潜在风险。

 吸引器
吸引器 高频电刀
高频电刀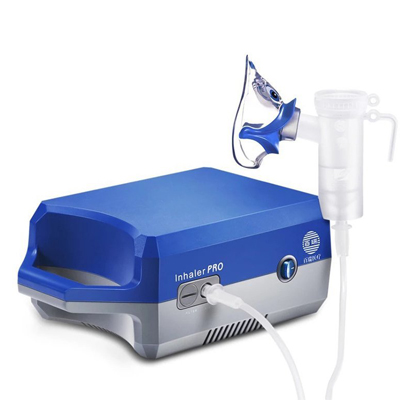 雾化器
雾化器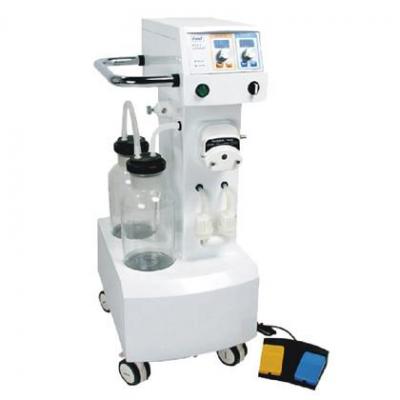 吸脂机
吸脂机 洗胃机
洗胃机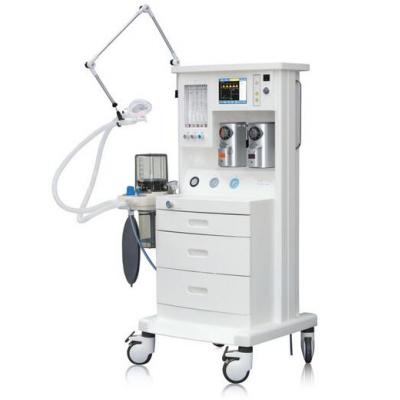 麻醉机
麻醉机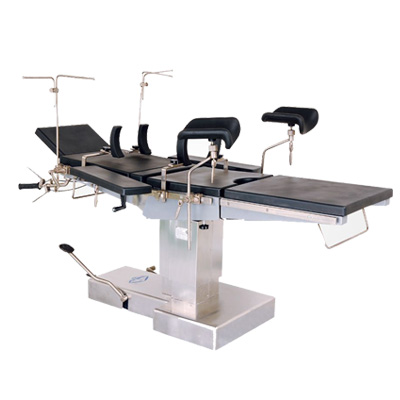 手术台
手术台 无影灯
无影灯